◆「赤い着色料」への不安から問い合わせ殺到
「紅麹と関係があるのでは」「大丈夫なのか」 問題発覚後、明太子メーカー「かば田食品」(北九州市)には消費者からそんな問い合わせが相次いだ。福岡を中心に50店舗を展開する大正時代創業の老舗。担当者は「お客さまには大変ご心配をいただきまして…」と言葉を濁す。 問い合わせ殺到の理由は、消費者が赤い着色料に不安を覚えたから。ウェブサイトに「『小林製薬製紅麹』は使用しておりません」と、同社と無関係であることを強調した文言を掲載し、ようやく沈静化した。
小林製薬の紅麹は使用していないと記した、明太子メーカー「かば田食品」のウェブサイト
全国辛子めんたいこ食品公正取引協議会(福岡市)の梅﨑了一事務局長は「最近では着色料を使わない明太子も多い。使っていても、紅麹の色素は一般的ではない」と断言する。 明太子のように、とんだとばっちりの事例もあるが、厚生労働省によると、小林製薬の原料を使っていた事業者は、直接同社から卸していた52社を含む計225社に上る。厚労省の飯塚渉・HACCP推進室長は「小林製薬以外、健康被害は確認されていない」と説明する。◆販売まで1年以上…幻の「濃厚チーズせんべい」に
ただ、実害を被った企業は少なくない。 「もう少し早く公表してくれていれば…」。健康食品の製造販売を手がける「ZERO PLUS」(福岡市)の担当者は苦言を呈する。 同社は問題が公になる1週間前の3月15日、「罪悪感の少ないお菓子やおつまみ」をキャッチフレーズに、小林製薬の原料を使用した新商品「悪玉コレステロールを下げるのに役立つ 濃厚チーズせんべい」を発売したばかりだった。
発売からわずか1週間で自主回収に追い込まれた幻の「濃厚チーズせんべい」=ZERO PLUS提供
原料は健康被害が出た製品ロットとは違ったが、新商品約700袋の多くを自主回収し、機能性表示食品の届け出も撤回した。「販売まで1年以上を費やした。パッケージのキャラクターも創作し、万全の準備をしていた」。今回、小林製薬が最初に健康被害を把握したのは1月だっただけに、電話口から恨み節が漏れる。 影響は、琉球王朝時代から珍重されてきた沖縄の伝統的発酵食品「豆腐よう」にも及んだ。◆豆腐ようもサブレも…広がる「停止」
「すぐに自主回収を決め、ウェブサイトで発信したが、お客さまに何かあったらと思うと気が気でなかった」と話したのは海洋食品(沖縄県浦添市)の池原昇・営業部長。こちらも問題の製品ロットとは違ったが、生産を停止した。「豆腐ようは島豆腐を泡盛などに漬け込んで、紅麹で発酵させるのに3〜4カ月かかる。別の原料を使っても販売再開には半年以上はかかる」と頭を抱える。 余波は企業以外にも。京都市の障害者福祉施設「西寺(さいじ)育成苑」では、小林製薬の原料を着色料に知的障害のある11人の利用者が作っていたサブレが販売停止に。籔田充施設長は「秋には紅葉、春には桜と季節に合わせて型を変えて、子ども食堂でも人気だった」と説明。「サブレの製造販売は利用者が購入客と接する機会で、充実感を得やすい。みんな、とてもショックを受けている」と続ける。 「こちら特報部」は他にも、小林製薬の原料を使用した事業者に取材を申し込んだが、「影響が甚大であまりにつらく、勘弁してほしい」と言葉が続かない老舗企業もあった。◆原因物質も特定できないまま
厚労省によると、小林製薬の紅麹問題を巡っては21日までに、延べ1459人が医療機関を受診し、247人が入院した。死者は5人に上り、同社には約9万2000件もの相談が寄せられている。 原因について、小林製薬は3月末、健康被害が報告された製品ロットや原料から、青カビ由来の「プベルル酸」が多く検出されたと公表した。だが、今月19日には厚労省が、プベルル酸のほかに未想定の物質が複数見つかったと公表。原因物質の特定さえ混迷しており、調査の長期化は避けられない状況となっている。 今回の問題は、機能性表示食品への信頼を揺るがしている。 消費者庁が19日に開いた機能性表示食品制度のあり方を巡る専門家検討会の初会合では、問題の小林製薬のサプリに、米国で医薬品として承認された「ロバスタチン」と同じ物質「モナコリンK」が含まれていることが議題に上がった。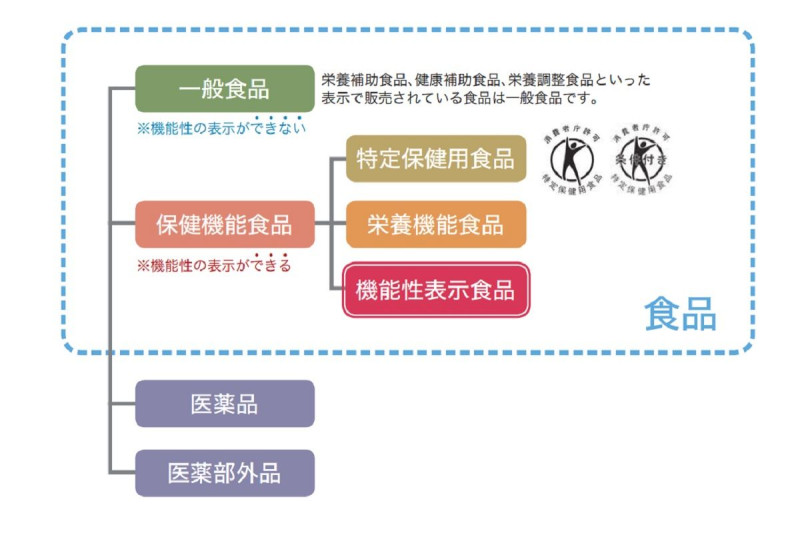
機能性表示食品や特定保健用食品などの分類(消費者庁のパンフレットより)
検討会に参加した国立医薬品食品衛生研究所の合田幸広名誉所長は「米国では医師の処方が必要な医薬品成分が入っている。大きな問題だ」と指摘。「品質管理の部分で、どういう形で国民の安全を守るか方向性を決めていくべきだ」と事業者任せの安全管理体制の見直しを求めた。 医薬品の場合、メーカーは、厚労省の省令に基づく製造・衛生管理の指針「GMP(適正製造規範)」の認証を得る必要がある。原料を含めたすべての製造工程で、複数の厳しいチェックが求められる。 錠剤やカプセル型などのサプリ製造については「推奨」にとどまっており、小林製薬が問題のサプリの原料を製造していた大阪工場(昨年末に閉鎖)は、GMPの認証を取得していなかった。◆安全性の「審査」は以前から課題だった
日本食品安全協会の長村洋一代表理事は「GMPが適切に導入されていれば、原料の製造過程で品質の異常に気づき、今回のような事態は防げた」との認識を示し、サプリ製造についてGMP取得を法律で義務付ける必要性を訴える。「医薬品成分が含まれていることを認めながら、GMPを義務づけないのは制度として落ち度がある」 機能性表示食品制度は、安倍政権が進めた規制緩和の一環で2015年に始まった。健康に寄与するなどといった「機能性」と有効成分の「安全性」は、事業者責任で科学的根拠を示せばよく、国が審査をしないことが、かねて制度の課題とされてきた。
「紅麹」の健康被害をめぐり、小林製薬が使用中止を呼びかけ、回収している商品
制度は法律ではなく、ガイドラインで運用され、被害報告も努力義務止まり。ガイドラインは「健康被害の発生及び拡大の恐れがある場合、消費者庁へ速やかに報告する」と規定しているが、報告までの期間は明示していない。小林製薬は最初の被害把握から報告まで2カ月超を要した。 消費者庁は今回の問題を受けて機能性表示食品を届けている約1700事業者を調査。16日までに計35製品、計147件の健康被害報告があったと明らかにした。ただ、小林製薬の事例を除いて事業者名や製品名は明らかにしなかった。◆「健康被害も氷山の一角ではないか」
市民団体「食の安全・監視市民委員会」の佐野真理子共同代表は「この制度は全て事業者任せでスタートしたのが特徴。報告義務がなく、今回明らかになった健康被害も氷山の一角ではないか」と指摘し、制度の抜本的見直しを求める。 「少なくともGMPと、健康被害の報告は法律で義務化し、行政は健康被害の恐れがある製品名を開示すべきだ。被害者救済制度の創設や、消費者を誤認させかねない広告の規制を含め、消費者を守る仕組みに改めないといけない」◆デスクメモ
小林製薬を巡っては、床にこぼれた材料を使って紅こうじ原料を作り、出荷した事例も明るみに出た。今回の健康被害とは直接関係ないが、衛生意識の欠如が疑われる話だ。医薬品でなければ管理が甘くていいのか。消費者目線に立ち、一連の問題の背景をしっかり検証してほしい。(北) 鄭重声明:本文の著作権は原作者に帰属します。記事の転載は情報の伝達のみを目的としており、投資の助言を構成するものではありません。もし侵害行為があれば、すぐにご連絡ください。修正または削除いたします。ありがとうございます。




